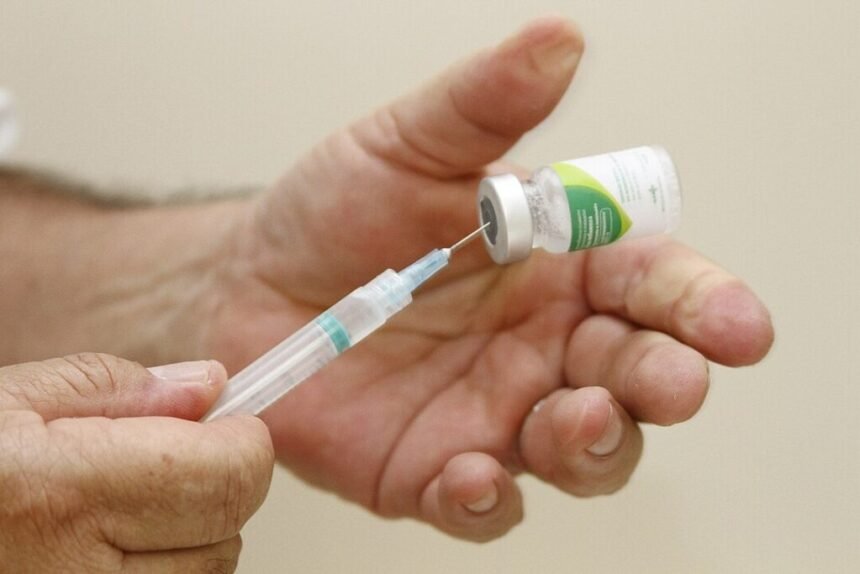
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou nesta terça-feira (1º) o início dos testes clínicos em humanos da primeira vacina brasileira contra a gripe aviária. Desenvolvido pelo Instituto Butantan, o imunizante utiliza a mesma tecnologia empregada na produção da vacina contra a influenza sazonal.
O projeto teve início em janeiro de 2023 e passou por uma etapa de testes pré-clínicos com animais, utilizando cepas vacinais fornecidas pela Organização Mundial da Saúde (OMS). O objetivo da pesquisa é preparar o Brasil para uma eventual pandemia causada por subtipos da influenza aviária, especialmente o H5N1, que apresenta taxa de letalidade de aproximadamente 50% em humanos.
O instituto informou que a vacina foi formulada com três cepas diferentes do vírus:
- Influenza A/Anhui/1/2005 (H5N1)
- Influenza A/Astrakhan/3212/2020 (H5N8)
- Influenza A/duck/Vietnam/NCVD-1584/2012 (H5N1)
Essas amostras foram enviadas por centros internacionais de controle de doenças, como o CDC (Estados Unidos) e o NIBSC (Reino Unido), em alinhamento com protocolos da OMS.
Embora casos em humanos sejam raros, especialistas brasileiros reforçam que o risco de disseminação global da doença existe, especialmente entre profissionais que trabalham em granjas. O Brasil, maior exportador de carne de frango do mundo, se declarou livre da gripe aviária em 18 de junho, após 28 dias sem registros em granjas comerciais.
Em maio deste ano, o único foco confirmado ocorreu em Montenegro (RS), e levou 16 países a imporem restrições temporárias à carne brasileira. Atualmente, apenas o Japão mantém limitações às importações de três municípios afetados.